- 超音波検査
- 超音波技術
- 初期の医学応用
- 原著論文
- 1952 Aモードによる腫瘍の良悪性の鑑別
- 1954 Bモードによる解剖学的構造の描出
- 臨床応用
- ・頭部
- ・産婦人科領域
- ・心臓
- 原著論文
- 1958 コンパウンド法による産婦人科エコー
- 1954 Mモードによる心臓エコー
- 関連文献
- 1980 アメリカ初期の超音波診断学
- 1974 産婦人科エコーの黎明期
- 技術的発展
- ・スキャンコンバーター
- ・電子スキャン
- ・ドプラ法
- 原著論文
- 1971 電子スキャン
- 1957 ドプラ法
- 1962 血流ドプラ現象の成因
超音波検査
超音波技術
1794年,イタリアの博物学者Lazzaro Spallanzaniは,コウモリに目隠しをしても飛べるが,耳を塞ぐと飛べなくなるという実験結果から,人間の可聴域外の音波,超音波の存在を予測した. 1880年,物理学者Pierre Curie(後にラジウムを発見) ,Jacque Curie兄弟は,ある種の物質を変形させると電荷が発生する現象,すなわち圧電効果(piezoelectric effect)を発見し,さらにその後,逆に結晶に振幅電位を加えると容積が変動することを発見した.これは初期からレコードのカートリッジ,マイクロフォンなどに応用されたが,後に超音波装置の送受信機,トランスデューサ(transducer)の基礎原理となった.
1912年,タイタニック号の沈没事故を契機として,氷山など海面下の障害物を発見する手段として超音波技術が注目を浴びた.1914年に勃発した第一次世界大戦では潜水艦が投入され,フランスの物理学者でかつてPierre Curieの学生だったPaul Langévinが超音波を利用した潜水艦探知技術を研究したが,これはその後第二次世界大戦中にアメリカでソナー(SONAR, Sound Navigation and Ranging)として実用化された.1928年,ソ連の物理学者Sokolovは,金属物体の一方から超音波を入力してこれを他端で検出し,物体内部に不均一があると超音波が減弱することを利用した非破壊検査法のひとつ,探傷装置(flaw detector)を開発した.この他第二次世界大戦ではレーダーも実用化され,これらソナー,探傷装置,レーダーなど媒体中の波動検出技術が,戦後の医用超音波技術の基礎となった.初期の研究者は,戦時中にこれらの技術の研究に従事していた者も多く,軍用物資を利用して試作された装置もあった.またCT,MRIなど他のモダリティと異なり,多数の研究者により同時多発的に様々な装置,検査法が開発されたことも初期の超音波研究の特徴のひとつである.

図1. Dussikらによる初の超音波の医学応用.頭部側面像.中央の黒い部分が側脳室であるとしているが,その後アーチファクトであることが指摘された[2].
初期の医学応用
初めて超音波の医学応用を試みたのは,オーストリアの医師Karl Dussik,物理学者のFriedrich Dussik兄弟とされる.1942年,Dussikらは,探傷法を応用して側頭部に超音波送信器,対側に受信器を置いて脳室構造を検出したと報告した[1,2](図1).彼らはこの方法を Hyperphonographyと称した.その後,彼らが脳室壁と見なしたのは頭蓋の反射であるとされその意義は否定されたが[3],超音波による非侵襲的検査への期待が高まる契機となった.この研究をふくめ,初期の超音波研究は頭蓋を対象としたものが少なくない.現在からみると奇異に思えるが,頭蓋内の情報を容易に得る手段がなかった当時,非侵襲的な頭蓋内検査が求められた機運は理解しうるところである.
1949年,米国海軍医学研究所の外科医George Ludwigは,超音波探傷装置を応用して実験的な胆石の検出に成功すると同時に,様々な組織中の音速を測定し,これはその後の研究の基礎データとなった[4]
1950年,ミネソタ大学の外科医John Wildと電気工学者のJohn Reidは,イヌの腸管壁の厚さをAモードで測定し,波形によって壁の層構造を識別できること,摘出胃癌標本で健常部と病変部の波形が異なる事を示し,腫瘍診断の可能性を示した[5].さらにWildらは,乳腺腫瘍の患者21名にこれを臨床応用し,良悪性の鑑別に有用であることを示した[→原著論文].Wildらの装置は,初の接触型探触子を使用したもので,これを Echoscope と称している.またAモードに加えて2次元Bモードの画像も提示している.

図2. Howry & Homesによる超音波検査装置Somascope.B29爆撃機の回転砲塔を利用した水槽で頸部を検査している [7].
1954年,コロラド大学の放射線科医Douglas Howryは,内科医のJoseph Holmesとともに,海軍のソナーの部品を利用した装置,Somascopeを組立てた[→原著論文].Howryらの方法は,被写体を水浸する方法で,初期は洗濯桶,家畜用の水桶などを使用した.その後,B29爆撃機の回転砲塔を利用して,水浸した患者の周囲を送信トランスデューサが360度回転すると同時に,受信装置が平行運動する装置を開発したが,これは初のコンパウンド機械走査方式であった[6,7](図2).1957年には,歯科用の椅子を半円状の水槽に固定し,トランスデューサが周囲を半回転する Pan-Scannerを開発した [8].
Howryらは,一貫して水浸法(water-bath method) を採用していたが,1965年にはイギリスのDonald(→原著論文)に続いて米国では初となるコンパウンド接触式スキャン(compound contact scan) を開発し[9],検査が煩雑な水浸法は姿を消した.しかし,1977年にオーストラリアのグループが広範囲を歪みが少なくスキャンできる水浸法をあらためて追求し,その変法としてウォーターベッドの内部に8個のトランスデューサを備え,ベッド上に腹臥した患者の横断像を自動的に撮影できる装置を開発した[10].Octosonの名前で市販されたが,当時既に実用化が進んでいた接触式電子スキャナに比べて高価かつ画質が劣ることから普及しなかった.
この磁気,ミネソタ大学のWild & Reidは腫瘍の検出を第一に考え,コロラド大学のHowry & Holmesは解剖学的な断層像を得ることを目的としている点でアプローチの方法が異なっているが,いずれもそれぞれの方法で医用超音波技術のパイオニアとしてその発展に大きく貢献した.
原著論文
《1952-Aモードによる腫瘍の良悪性の鑑別》
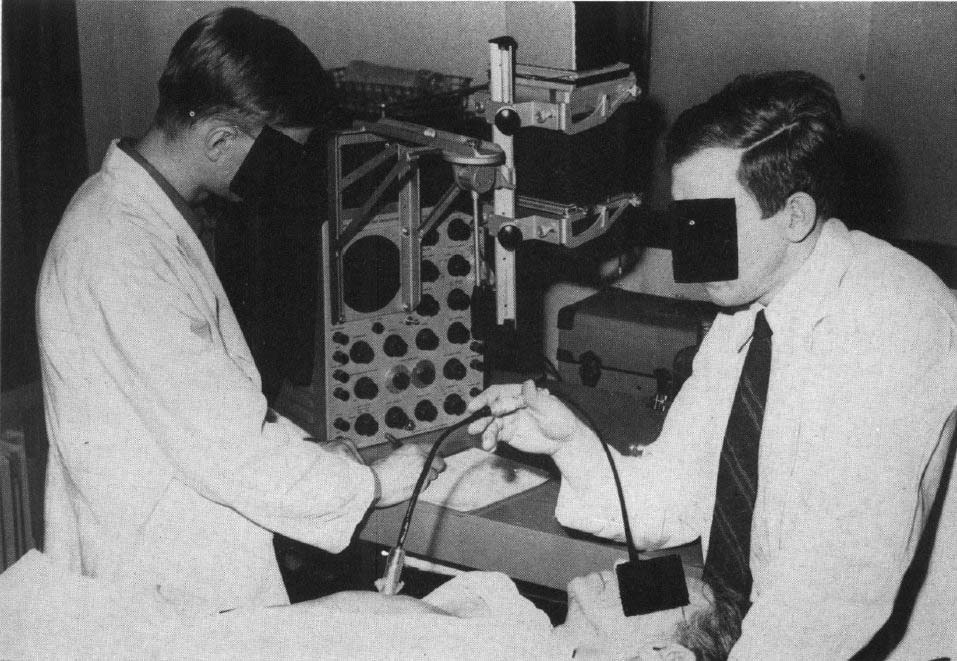
図3.患者の乳腺にEchoscopeを聴診器のように当てて検査している.
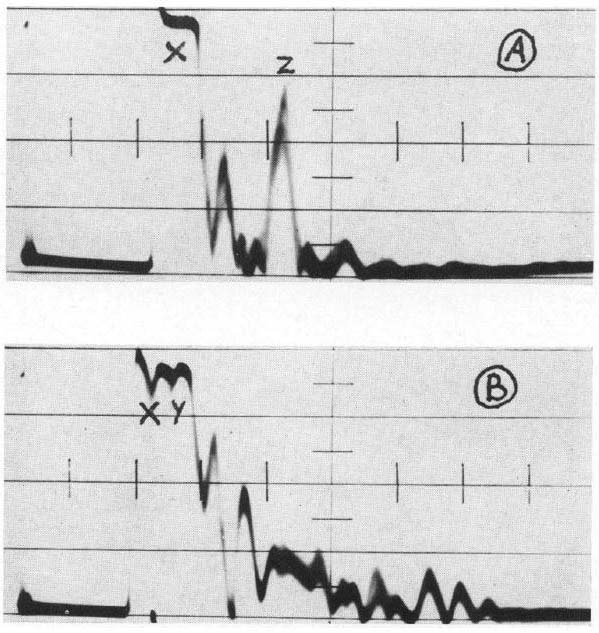
図4.乳腺のAモード波形.上は正常例,下は乳癌.波形の違いから良悪性の鑑別が可能であるとしている.
【要旨・解説】コロラド大学の外科医Wildと,電気工学者Reidのチームは,1950年以来,戦時中に開発されたレーダー観測トレーニング用の超音波装置を流用した超音波検査装置を開発し,実験を続けていた.最初は脳標本,次いでイヌの腸管,胃癌切除標本[5]にAモードを適用し,その臨床的有用性を示唆したが,本稿では初めて乳癌臨床例に適用し,良悪性の鑑別に有用であることを示した.
探触子は,水を満たした小さな容器の一端に圧電クリスタル,他端をコンドームの薄いゴム膜で閉鎖したもので,探触面は径9mm,それ以外に詳しい寸法の記載がないが,写真でみるとちょうどペンライト程度で,ゴム膜面を皮膚に接触させる.Stethoscope(聴診器) にならって Echoscope(エコスコープ)の名称を提案しているが,まさに聴診器を当てるようにして検査している(図3).超音波は,周波数15MHzのパルス波で,Aモードの波形をオシロスコープに表示する(技術的詳細については別項に記載されている[11][12]).
乳腺術前21症例に検査を行ない,良悪性の判定についてエコー所見と病理所見を対比した.診断方法は,病変部と健常部の波形を目視的,数値的に比較する方法で,エコーピークの数,輝線下面積,エコー強度などを検討した結果,輝線下面積が悪性腫瘍の診断に有意に有用であった(図4).腫瘍病変のエコーが正常と異なる理由として,細胞核の濃度が高いためではないかと推測している.
なにぶんにもAモードの波形による診断なので,個々の波形の解釈はほとんど不可能であり,このような形のエコー診断がこれ以後臨床に供されることはなかったが,超音波による臨床診断の可能性を初めて示唆した点で重要な研究であった.最後に付け足しだが,Bモードの2次元画像が提示されている.
Wild & Reidは,水浸法を採用したミネソタ大学のHowry & Holmesのチームと異なり,当初より接触法を採用しているが,これは解剖学的断層像の描出を主眼とするHowryらに対して,Wildらが腫瘍の診断,良悪性の鑑別を第一目標としていることから,必然的なアプローチであったといえよう.
超音波の生体に及ぼす副作用については,低周波数,高エネルギー,長時間の超音波が,熱生成,キャビテーションなど生体に影響を及ぼすことが知られているが,ここで使用するような高周波,低エネルギー,パルス状の短時間の照射では先行事例がない.そこで,動物の脳に照射したり,著者の上肢に30分間照射するなどの実験を行なったが問題がなかったとしている.
《1954-Bモードによる解剖学的構造の描出》
66:208-23,1954

図5.水浸式のSomascope.左側の大きな水槽に患者を入れて検査する.
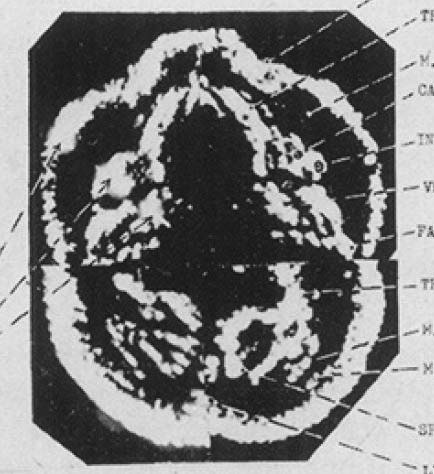
図6.頸部のBモード横断面像.
【要旨・解説】医用超音波画像のパイオニア,コロラド大学の放射線科医Douglas Howryと内科医Joseph Holmesのグループの論文である.腫瘍の検出を主眼とするミネソタ大学のWildらと異なり,彼らの目標は解剖学的な断層像の表示にあり,早期からBモードによる断面像を追及して1949年以来ソナーの部品を利用した装置Somascope(ソマスコープ)を試作していた.ここでは切除標本に加えて初めて臨床画像が提示されている.周波数など技術的な詳細は記載されていないが,水浸法によるコンパウンド走査である.装置の外観は,現在からは考えられないほど大がかりである(図5).画像はオシロスコープ画面に表示され,これを直接観察したり,あるいは写真機で撮影する.
乳癌の切除標本,健常人の頸部(図6),肝硬変,肝転移の症例が供覧されている.低解像度の二値画像(bistable)で,まだまだ臨床診断に役立つレベルではないが,正常乳腺や正常肝組織は均一な無エコーで,癌病変部には,健常部にないエコーが見られることから,臨床診断の有用性が示唆されている.びまん性疾患,多発転移では全体が不均一な高エコーとなり,「スノーストーム」状と記載されている.深部に位置する膵の描出は難しいとしている.
ここでは家畜用の水桶(cattle tank)を水槽として使用しており(図1),側面を探触子が平行移動するが,この方法では図2のような断面像は1回では描画できないため,4回に分けて描画して合成している.この問題を解決するために,その後1959年にはB29爆撃機の回転砲塔を利用して探触子が周囲を回転運動する装置を製作している(図3). 臨床応用にむけての課題として,分解能の向上とともに水浸法の煩雑さを挙げて,水槽を使用しない方法の必要性について触れているが,この後直接接触法を開発している[9].
臨床応用
1950年代は,この他にも各分野で様々な新しい試みが行なわれた.
頭部
スウェーデンのルンド大学のLars Leksellは,探傷装置を乳児の頭部にあてて正中構造の偏位から頭蓋内血腫を診断した[13].その後も超音波による頭蓋内病変描出の試み(echoencephalography)は続いたが[14],小児ではある程度の成果が得られたものの成人では頭蓋が障壁となって成果が得られず,やがてCTの登場で過去のものとなった.
産婦人科領域
1955年,英国グラスゴーの産婦人科医Ian Donaldは,子宮筋腫と卵巣嚢腫の切除標本を企業の研究施設にもちこんで探傷装置を利用して超音波画像が得られることを確認し,産婦人科領域への応用の端緒を開いた[15].しかし,当時一般的だった水浸法は特に妊婦の検査には使用しにくいことから,1957年に多関節アームの先端につけたトランスデューサを患者の腹壁に直接接触させて動かすコンパウンド式接触スキャナ(compound contact scanner)を開発した.これは初の水浸不要の接触スキャナであった[→原著論文].Donaldはこのほかにも,初めて胎児の児頭横径(BPD)を測定したり,検査前に膀胱を充満させる full-bladder techniqueを開発するなど,産婦人科領域における超音波検査の適応拡大に大きく貢献し[15,16],超音波検査は産婦人科領域で最も早く一次検査としての地位を固めるにいたった.
心臓
1954年,スウェーデンの循環器内科医Inge Edlerと物理学者Hellmuth Hertzは,Siemens社の探傷装置 Reflectoscope を利用して,初めて心臓の超音波検査法を報告した.各心腔の壁がエコーとして捉えられることを確認し,さらにその動きを連続的に動画に記録する,現在でいうMモードの技術を発明した [→原著論文][17].アメリカでは,ReidらもEdlerの方法を追試し,1963年に発表した論文 [18]はアメリカにおける心エコー研究の引き金となった.1965年,Harvey Feigenbaumらは,Mモードの心嚢水腫の診断における有用性を示したが[19],循環器病学における超音波の有用性については疑念も多く,臨床で広く利用されるようになったのは1970年代後半であった[20].1971年にBomが電子式走査[→原著論文]による2次元Bモード法を開発すると,イリノイ大学のEggletonらがこれを心臓に応用し[21],1980年代にはドプラ法も導入され,心エコー法に必要な基本的な技術が整った.
原著論文
《1958-コンパウンド法による産婦人科エコー》
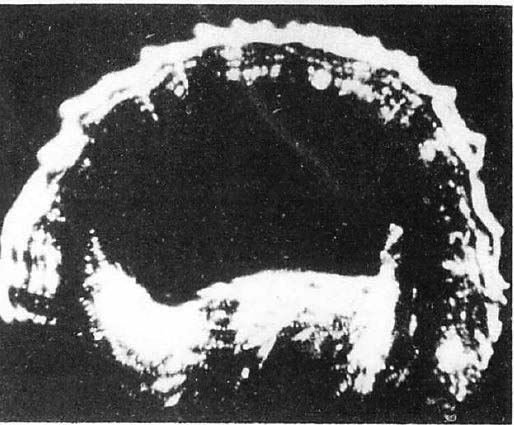
図7.大きな卵巣嚢胞.半円状の輪郭は腹壁.嚢胞壁の後壁が脊柱,後腹壁により陥凹している.
【要旨・解説】腹部腫瘤の超音波診断の可能性を初めて示した重要な論文である.市販の工業用超音波探傷装置を利用したBモード法であるが,電位計(potentiometer)を利用したPPI(平面位置表示装置)を組合わせて探触子の位置と方向を検出することによりコンパウンド走査を実現している.具体的には,探触子を腹部に密着させ,細かく首振りしながら腹壁に沿ってゆっくり手動で動かして水平断面を得る.先行研究のように,水槽が不要なのでより広い範囲が検査できるとしている.水浸法によらないBモード像の報告はおそらくこれが初報である.
著者のDonaldは英国グラスゴー大学の産婦人科医なので,症例は卵巣嚢胞(図7),子宮筋腫,妊娠子宮である.提示されている画像は,非常に粗い二値画像で,腫瘍や胎児の輪郭が辛うじてわかる程度で,著者もまだ装置は未熟であり,臨床に供するレベルに達していないと結論している.しかし,嚢胞性か充実性かの鑑別にはある程度役立ち,腹水を伴う胃癌と診断されていた患者が,超音波検査で卵巣嚢胞と判明した症例,子宮筋腫の術前検査で,妊娠していることが明らかとなった症例などが紹介されている.
超音波の有害作用については,Wildらと同様,やはり熱生成やキャビテーションが問題となりうるとして検討している.仔ネコの脳に1時間超音波を照射する実験を行ない,実験群,対照群,わずか2匹ずつではあるが,診断に利用する超音波の30倍以上の強度を照射しても組織学的に異常がなかったとしている.
現在では,腹部は超音波検査の最も良い適応のひとつであるが,表在臓器や心臓と異なり,周囲に腸管ガスが多く,臓器が深い位置にある腹部は,当時はもっとも challengingな分野であった.そのような中にあって,本論文は腹部超音波検査の可能性を示し,その後の発展のきっかけとなった点で重要な研究である.
《1954-Mモードによる心臓エコー》
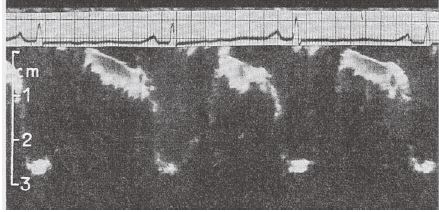
図8.僧帽弁狭窄.ここでは左房壁のエコーとされているが,その後僧帽弁前尖であることが判明した.
【要旨・解説】心臓超音波検査を初めて報告した重要な論文.Inge Edlerは,スウェーデンのルンド大学の循環器内科医で,心臓外科症例の術前検査を担当していた.共同研究者のHellmuth Hertz*は同大学の物理学者.当時市販されていたSiemens社の非破壊超音波探傷装置 Reflectoscope (リフレクトスコープ)を心臓の検査に応用した.
* Hellmuth Hertz (1920-85): ドイツの物理学者.超音波の研究のほか,インクジェット技術の開発でも知られる.父は物理学者 Gustav Hertz (1925年ノーベル物理学賞受賞),大叔父は周波数の単位に名が残る物理学者Heinrich Rudolf Hertz.当時,父のGustav Hertzは,Reflectoscopeを開発したSiemens社の研究所長であった.
リフレクトスコープの探触面は径12mmで,これを直接皮膚に当てて検査している.周波数は2.5MHzである.まず予備実験として,摘出心臓で各心腔と壁の境界面がAモードの波形として捉えられることを確認した.ついで臨床例に応用し,左第3~4肋間の左胸骨縁にスコープを当てると,正常例では9~11cmの位置に後壁が見え,心拡大があるとこの距離が増大することがわかった.
さらにAモードの波形を表示するオシロスコープの画面の前に幅5mmのスリットを設けてこれ映画カメラで撮影することにより,輝線の動きを連続的に時間軸上に記録する方法を考案した.著者はUCG(ultrasonic cardiography,超音波心臓図)と名づけているが,これは現在のMモード法に外ならない.心電図との同時記録も行なわれている.ここでは,正常例,大動脈弁閉鎖不全症,僧帽弁狭窄症のUCGが提示され,左室後壁,左房後壁の動きが論じられている.しかし,ここで左房壁とされていたエコーは,その後僧帽弁前尖であることがわかり[22](図8),以後Edlerは特に弁膜症における弁尖のMモード波形の研究を続け,例えばその後僧帽弁狭窄症の重要な診断指標となった僧帽弁前尖後退速度に関する知見も既に明記している[23].Edler自身は,1969年にDoppler法の報告を最後に心エコーの研究を行なっていないが,以後超音波検査は循環器疾患の検査手段として必須のものとなり,Edlerは心臓超音波検査の父とされる.
関連文献
《1980-アメリカ初期の超音波診断学》
【要旨】第二次世界大戦中に発達した金属探傷器,ソナーの技術を下に,1940年代のアメリカで3人の研究グループが独立に超音波の医学応用の研究を開始した.
ペンシルベニア大学のLudwigは組織中の音速測定を行なった.コロラド大学のHowryは,B29爆撃機の砲塔を利用した水浸法スキャナを試作し,コンパウンドスキャンで人体の横断像を描出し,その後著者のHowryも加わって半円形の水槽を使ったパンスキャナを作った.ミネソタ大学のWildは,Aモードによる腸管壁の計測からスタートし,Aモードによるエコーパターンの違いから,乳癌の良悪性を診断する方法を開発し,組織の特性診断を研究した.
イギリスでは,1955年からグラスゴーの産婦人科医Donaldが研究を開始し,1957年に接触式コンパウンドスキャンを開発して,婦人科腫瘍,妊娠の診断法を発展させた.
脳の超音波診断は,1942年に発表されたオーストリアのDussikの研究に刺激されたマサチューセッツ工科大学のBolt,マサチューセッツ総合病院のBallantineが研究を進めたが,1950年に頭蓋による減衰を克服できず断念した.1955年,スウェーデンのLexellは,正中構造の偏位の診断に成功した.イリノイ大学のFryは,高出力の超音波で神経組織を破壊して神経機能の変化を調べた.これを利用して,1957年にアイオワ大学のMeyerらはパーキンソン病の治療を試みた.
眼科領域では,フィンランドのOksalaがAモードによる眼球内異物の診断,ニューヨークのBaumがBモードコンパウンドスキャナによる腫瘍の描出を報告した.
心臓エコーは,スウェーデンのHertz,Edlerが探傷器を利用して心臓の運動パターンを研究し,僧帽弁前尖の特徴的な所見を確立して以後,心臓エコーが発展した.日本は,1950年代にドプラ法の開発で欧米に先行し,多くの日本人研究者が心臓エコーの発展に貢献した.
【解説】本稿は,1952年に創設された米国超音波医学会(AIUM)の25周年に際して,その創設者のひとり,Holmesが学会の初期10年間の歴史を振り返ったものである.医用超音波開発史の特徴のひとつは,特定の「発明者」 がなく,多くの研究グループにより同時多発的に研究が進んだことである.
最初期の米国内研究グループとして,ペンシルベニア大学のLudwig,コロラド大学のHowry,ミネソタ大学のWildが挙げられているが,その後現在にいたる臨床超音波診断学の流れを作ったという点では,Howry, Wild,および英国のDonaldが三大パイオニアであったといえよう.著者のHolmesは,Howryのグループの一員である.各グループは,それぞれ他のグループの研究を知りながらも,それぞれ独自のアプローチで思うところを追求しているが,最後に述べられているように,現在臨床に広く用いられている超音波技術のほとんどすべてが,1950年代に彼らにより試みられていた.
当時の装置の写真が数多く掲載されているが,いずれも大がかりである.超音波診断装置は,画像診断機器発展の歴史の中でも,最もコンパクト化が進んだものといえよう.ベッドサイドで手軽に使える装置を見慣れている目から見ると,技術の進歩を実感するところである.
《1974-産婦人科エコーの黎明期》
【要旨】1955年,スコットランド,グラスゴー大学の産婦人科医の著者は,子宮筋腫と卵巣嚢腫を近隣の工場に持ち込み,超音波金属探傷器を借りて実験したところ,充実性腫瘍と嚢胞性腫瘍で明らかにエコー像が異なることからその可能性を知った.当時,アメリカのWild & Reidが被写体を水槽にいれる水浸法で超音波の腫瘍診断における有用性を報告していたが,水浸法は臨床に応用しにくいことから,企業の協力を得てコンパウンド式接触スキャナを開発して臨床に応用した.ある時,著明な腹部膨満があり,胃癌の播種による腹水と診断されていた患者を検査したところ,巨大な卵巣嚢胞腺腫であることがわかり無事摘出できたことから,臨床的有用性を確信した.
その後腹部超音波検査が急速に普及したことは,産科領域での発展に負うところが大きい.児頭大横径(BPD)の測定,胞状奇胎,流産,前置胎盤,双胎などの診断に有用である.
あるとき偶然,長く待たせた患者の膀胱が充満状態で検査したところ,腸管が圧排されて子宮が非常に良く見えた.
安全性は常に最優先の課題であった.1970年に南アフリカの研究者が,超音波による染色体損傷の可能性を指摘した.その後自他の施設での実験でこれは否定されているが,今後さらに新しい装置の開発にあたっては常に注意が必要である.
【解説】産婦人科エコーの可能性を初めて実証し,その後の腹部エコーの発展を導いたイギリスの産婦人科医Donaldが,ユーモアに富む砕けた語り口で自らの研究歴18年を振り返った英国外科学会での講演記録である.腹部は腸管ガスのため検査が難しい領域であったが,1958年のDonaldの論文[→原著論文]がその臨床的有用性を証明して以降,腹部超音波は急速に発展した.骨盤臓器の検査における膀胱充満法(full bladder technique)を紹介したのもこの論文である.技術的には,水浸法に代えて直接接触法によるコンパウンドスキャンを初めて成功させた点が最大の功績である.当初水浸法を採用していたアメリカのHolmesらも,その後この方法を採用している[9].
画像はまだ二値画像(bistable image)であるが,1枚だけグレイスケールの現状を示す画像が供覧されており,将来展望の項では,グレイスケールの進歩,開発中の3次元画像について触れている.
技術的発展
スキャンコンバーター
1950年代の超音波検査は,基本的にBモードによる2次元画像が主体であったが,いずれもオシロスコープ上の画像を記録するもので,白黒二値画像(bistable image)であった.オシロスコープのゲインを調節して複数の画像を重ね合わせるなどして擬似的にグレイスケールを表示する工夫はあったものの,臓器の輪郭はわかっても内部構造はほとんど見えなかった.
本格的なグレイスケール画像は,受信した超音波信号を直接オシロスコープに入力するのではななく,電子回路で処理して画像表示装置に送るスキャンコンバーターが登場して初めて可能となった.これはコンパウンド接触スキャナの登場と並び,超音波検査技術上の大きな飛躍であった.
電子スキャン

図9.1976年発売,国内初の電子スキャン装置「エコーカメラ」(アロカ社).まだラックいっぱいの大型装置であった[44]
最初期のBモード2次元スキャンは,探触子直下のビーム幅領域に限定されたsingle scanであった.その後探触子を体表面上で移動させ,これにポテンシオメータを利用した平面位置表示器(PPI, plan position indicator)を組合わせることにより,広範囲を描画できるコンパウンドスキャン(compound scan,複合走査)が登場した.探触子の移動法は,手動あるいは機械式であったが,手動の場合は相応のコツが必要で,いずれにせよゆっくりと移動させる必要があり,このような低速スキャンで得られる画像は静的画像であった.
リアルタイムに動的な画像を得るための高速スキャン法としては,初期は探触子内で単一の圧電素子を往復させる機械式走査であったが,現在主流となっている多数の圧電素子をならべて電子的にスイッチングしながら走査する電子スキャンは,1967年にオランダのJan C. Somerがフェイズドアレイ方式[24],その後1971年にNicolaas Bomら[→原著論文]と,日本の入江喬介(アロカ社)がリニア方式をほぼ同時に完成し[25],これによって実用的なリアルタイムの検査が可能となった.しかし,まだこの時代は大きなラックいっぱいの各種装置が必要(図9),ベッドサイドで使える小型の装置が各メーカーから市販されたのは1980年代であった.
ドプラ法
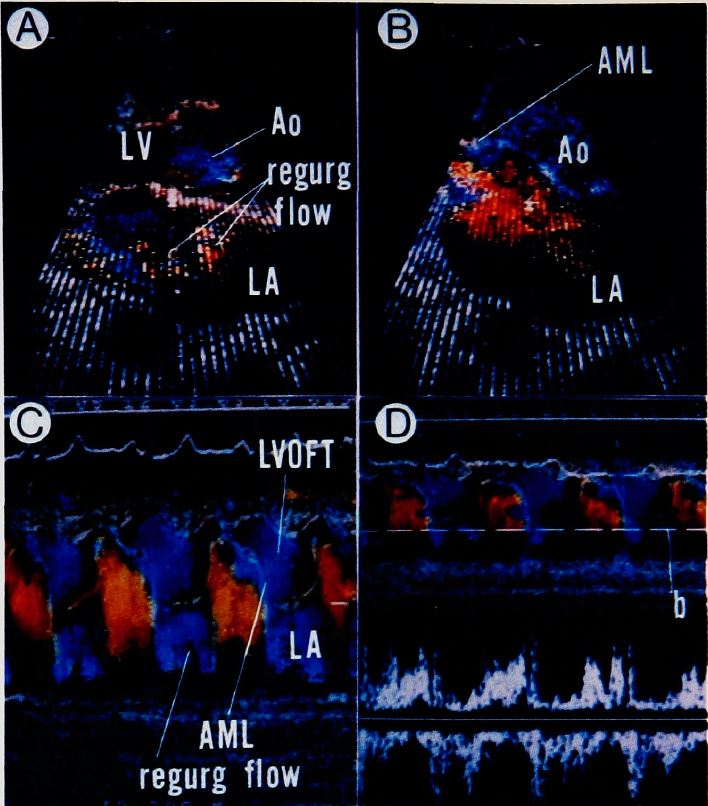
図10.心臓のカラードップラー法 [37]. 近づく血流を赤,遠ざかる血流を青で表示する.
1842年,オーストリアの物理学者Christian Dopplerが,移動する物体が反射する波の周波数が変化する現象を発見し,これはその後ドップラー効果と呼ばれた(医学分野では「ドプラ」と記載することが多い).超音波検査にこれを初めて応用したのは,1956年,里村茂夫(大阪大学理工学部),仁村泰治(国立循環器病センター)らである[→原著論文][27],当初の対象は心臓,特に弁膜の動きの検出にあったが[28],その後里村は金子仁郎(大阪大学精神科)とともに血流診断にこれを応用した[29,30].
血流から得られるドプラ信号の成因については,里村は当初乱流と考えていたが,大阪大学の加藤金正はこれが赤血球によること,そのエネルギーが単位体積当たりの赤血球数に比例することを示し,これはその後のドプラ血流計測の基礎となった[→原著論文].欧米でも末梢血管[31,32],心腔内血流[33]の診断における有用性が報告された.しかしいずれもドプラ信号の波形,振幅による評価であるため,特に心腔内のように流れが複雑な部位の評価は難しかった.
1981年,アメリカのBrandestiniらが,ドプラ信号を血流の方向と速度に応じたカラー画像で表示するカラードプラ法を報告した[34].しかしこれはMモードあるいはBモードの画像を表示後,ドプラモードに切替える必要があった.現在のようなリアルタイムカラードプラ法を初めて実現したのは,日本のアロカ社(その後日立にメディコに吸収合併)の滑川孝六を中心とする研究開発チームで,1982年の第3回世界超音波医学会で発表[35],その翌年に製品化され,共同研究者の尾本良三(埼玉医科大学外科)のアトラス出版も手伝って国内外に広く普及した*[36,37](図10).現在では,心血管領域のみならず,全身の腫瘤性病変の血流評価にも欠くことのできない検査法となっている.
*カラードプラのカラー表示は,Brandestiniの初報では探触子に近づくフローが青,遠ざかるフローが赤で表示されていた.物理学的には,観測者から遠ざかる物体からの反射光は波長が延長して赤色側に偏位するので自然な選択であった.しかしその後,国内外に広く普及したアロカ社の製品はこの逆で,探触子に近づくフローが赤で表示された.この結果,近づくフローを赤くするBART(blue away red toward)表示,青くするRABT(red away blue toward)表示が混在する結果となった[38].1990年代に,国際学会でこれを統一しようとする動きがあったが[39],アロカ社が譲らず現在に至っている.アロカ社が近づくフローを赤にした理由については,共同研究者の尾本良三が「議論の余地はない.近づいてくるというのはパッションで,"情熱"を意味する.情熱は赤だ! 遠ざかるものは離れていくのだから,寂しくブルーだ!」と言ったからだという[40].
原著論文
《1971-電子スキャン》

図11.20素子を備えた電子スキャントランスデューサ.
【要旨・解説】1970年以降,主流となり現在に至る電子スキャン法普及の端緒となった,オランダの技術者Bomらによる論文である.電子スキャン法はこれ以前にも,1965年にドイツのBuschmann[41]が眼球用探触子を開発し,1968年にSommer[24]が装置の構造について報告しているが,体部への臨床応用に関してはこの論文が初報である.これ以前は,Bモード像を得るには,探触子を手動あるいは機械的に体表をゆっくり移動させる必要があり,心臓のように動きのある構造を描出することは難しかった.著者らは,圧電素子を20個ならべ,これを電子的にスイッチングすることにより,心臓の動きをリアルタイムに描画することができる装置を開発した.
個々の素子は径3mmの円板状で,これを1列に20個ならべて幅約6cmのマルチアレイ探触子を使用している(図11).実験用なのでみかけは粗造りだが,現在の装置とほぼ同じ形状である.フレームレートは190/秒,周波数3Mzである.大動脈の摘出標本の画像が掲載されている.奥行き方向の空間分解能が4mmであるため非常に粗い画像であるが,輪郭が明瞭に描出されている.臨床例は掲載されていないが左心室の壁を描出できたとしている.
表題にもあるように,このような方式を開発した目的は,心臓の動きを観察することにあったが,その後,心臓以外の領域で圧倒的に普及することになった.
《1957-ドプラ法》
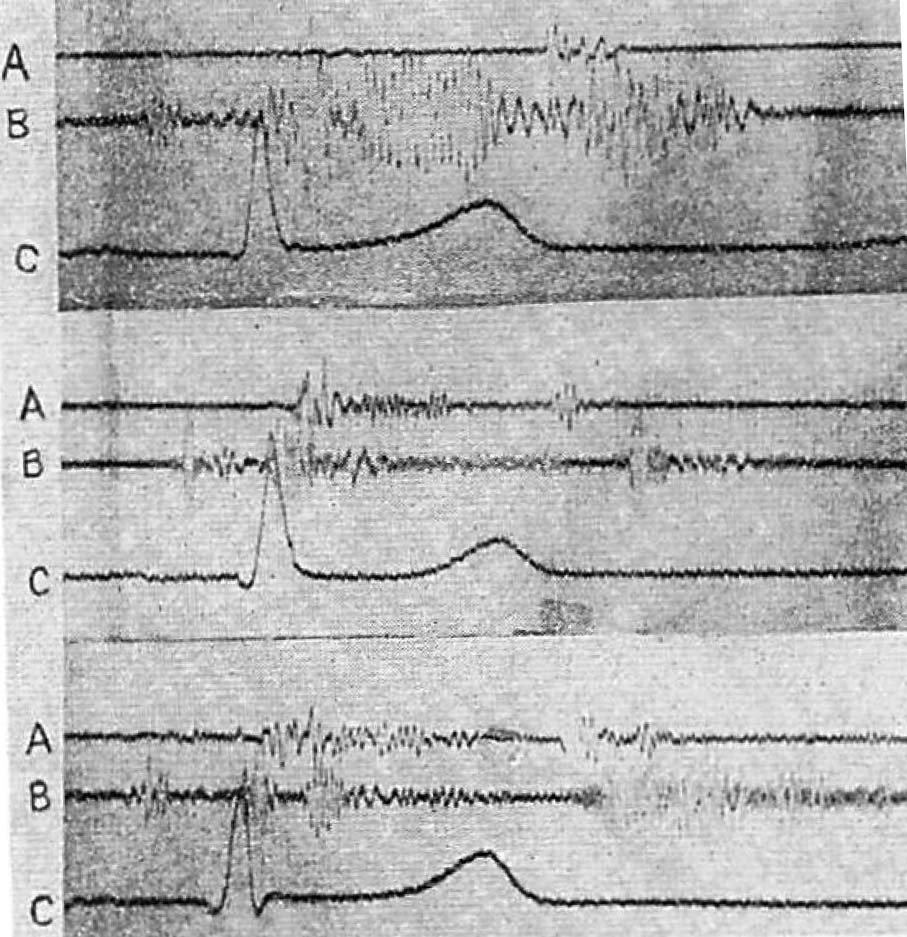
図12.上から低周波ドプラ信号,高周波ドプラ信号,ドプラ心雑音.A:心音,B:ドプラ信号,C:心電図
【要旨・解説】ドプラ現象を医学に初めて応用した画期的な論文である.著者の里村茂夫は物理学者であるが,早くからドプラ効果の振動現象への応用に関心をもって研究をすすめ,そのひとつとして医学応用の可能性も念頭においていた[26].これを知った大阪大学の循環器内科医仁村泰治が共同研究を持ちかけたのが,ドプラエコー法研究の始まりであった[43].ここでは,動物実験および臨床例で,ドプラ信号を心音図,心電図と同時にオシロスコープ上に表示した(図12).異なるフィルターを使用することにより,低周波ドプラ信号(500Hz以下),高周波ドプラ信号(約1000Hz) が得られ,それぞれ心臓壁の運動,弁膜の運動に対応すると考えられた.また,フィルターを使用しない状態では,異常な心臓で聴診される心雑音に対応するドプラ心雑音が得られた.その後,里村は共同研究者の仁村とともにさらに症例を重ねて,本法による弁膜運動の評価が弁膜症や高血圧心の病態評価に有用であることを続報している[28].
ここで着目しているのは心臓壁と弁膜の運動で,現在ドプラ法の主たる活躍の場である血流診断については論じられていないが,里村は本稿でドプラ心雑音と表現されている高周波成分が血流によるものと推測し,その後金子仁郎らとともに血流ドプラ検査を開発した[29,30].
里村は,大阪大学理工学部の物理学者でドプラ現象の医学への応用を着想し,循環器内科医の仁村泰治の協力を仰いでドプラ超音波法を開発した.本稿は里村の単著で,仁村については謝辞にその名前が見えるのみであるが,これについてはその後仁村が当時の複雑な事情を回想している[42].
《1962-血流ドプラ現象の成因》
【要旨・解説】1957年,里村茂夫による心臓ドプラエコー法の初報は,主に心臓壁, 弁膜の運動に着目したものであったが,この時すでに血流からもドプラ信号が発生していることに気付いており,その成因は血液の乱流であると考えていた[29].1960年,里村の急逝後,大阪大学のドプラエコー研究チームで物理学分野の研究を継承した加藤金正は,これが血球によるものと考えた.
血液の流れは,里村のいうように乱流ではなく,基本的に層流である.指尖の細い動脈からもドプラ信号が得られるが,この程度の遅い流速で乱流が起こることは考えられない.これらのことから,加藤は血球による音波の反射がドプラ信号の原因であると考えた.これを証明すべく,澱粉溶液およびウシの血液を使って実験し,信号強度が粒子数の平方根に比例すること,流速には依存しないことを示し,さらに理論的にこれを証明したのが本稿である.背景にあるのは,粒子の直径に比して音や光の波長が十分長いときに起こるRayleigh散乱である.
出典
- 1. Dussik KT. Über die Möglichkeit, hochfrequente mechanische Schwingungen als diagnostische Mittel zu verwerten.Zeitschrift gesamte Neurologie und Psychiatrie174:153–168,1942
- 2. Dussik KT, Dussik F. Auf dem Wege zur Hyperphonographie des Gehirns. Wien Med Wochenschr 97:425-9,1947
- 3. Guettner W. Über Ultraschallabbildungen am menschlichen Schädel. 2:148-56,1952
- 4. Ludwig GD.The velocity of sound through tissues and the acoustic impedance of tissues. J Acoust Soc Amer 22:862-6,1950
- 5. Wild JJ. The use of ultrasonic pulses for the measurement of biologic tissues and the detection of tissue density changes. Surgery 27:183-8,1950
- 6. Holmes JH, Howry DH. Ultrasonic visualization of edema. Trans Am Clin Climatol Assoc 70:225-35,1959
- 7. Homes JH. Early diagnostic ultrasonography. J Ultrasound Med 2:33-43,1983
- 8. Holmes JH, Howry DH. Ultrasonic diagnosis of abdominal disease. Am J Digest Dis 8:12-32,1963
- 9. Holmes JH, Meyer EP, Posakony GJ, Howry DH. Ultrasonic contact scanner for diagnostic application. Am J Med Electron 4:147-52,1965
- 10. Carpenter D, Kossoff G, Garrett WJ, et al. The UI Octoson - A new class of ultrasonic echoscope. Aust Radiol 21:85-9,1977
- 11. Reid JM, Wild JJ. Ultrasonic ranging for cancer diagnosis. Electronics 25:136-8,1952
- 12. Wild JJ, Reid JM. Application of echo-ranging techniques to the determination of structure of biological tissues. Science 115:226-30,1952
- 13. Leksell L. Echoencephalography: Detection of intracranial complications following head injury. Acta Chir Scand 110:301-15,1955/1956
- 14. de Vlieger M. Ultrasound for two-dimensional echoencephalography. Ultrasonics 1:148-51,1963
- 15. Donald I. Aplogia: how and why medical sonar developed. Ann Royal Coll Surg Eng. 54:132-40,1974
- 16. Donald I. Clinical applications of ultrasonic techniques in obstetrical and gynaecological diagnosis. Br J Obstet Gynaeol 69:1036,1962
- 17. Edler I. The diagnostic use of ultrasound in heart disease Acta Med Scand Suppl 308:32-36,1955
- 18. Joyner CR Jr, Reid JM, Bond JP. Reflected ultrasound in the assessment of mitral valve disease. Circulation. 27:503-511,1963
- 19. Feigenbaum H, Waldhausen JA, Hyde JP. Use of ultrasound in the diagnosis of pericardial effusion. J Am Med Assoc 181:711-4,1965
- 20. Feigenbaum H. Evolution of echocardiography. Circulation. 83;1321-27,1996
- 21. Eggleton RC, Feigenbaum H, Johnston KW, Weyman AE, Dillon JC, Chang S. Visualization of cardiac dynamics with real-time B-mode ultrasonic scanner. In: White D, ed. Ultrasound in Medicine. Plenum Publishing Corp, 1975
- 22. Edler I, Gustafson A, Karlefors T, Christensson B. Ultrasound cardiography. Acta Med Scand 370:5-123,1961 Suppl.
- 23. Edler I, Gustafson A, Karlefors T, Christensson B. Mitral and aortic valve movements recorded by an ultrasonic echo-method. Acta Med Scand 370:67– 82,1961
- 24. Somer JAC. Electronic sector scanning for ultrasonic diagnosis. Ultrasonics 6:152-9,1968
- 25. Somer JC. The history of real time ultrasound. International Congress Series 1274:3-13,2004
- 26. Satomura S, Matsubara S, Yoshioka M. A new method of mechanical vibration measurement and its application. Memoirs Inst Scien Indust Res Osaka Univ 13:125-33,1956
- 27. Nimura Y. Short history of the development of echodardiography with special reference to that in Japan. J Echocardiogr 1:46-59,2003
- 28. Yoshida T, Mori M, Nimura Y, et al. Analysis of heart motion with ultrasonic Doppler method and its clinical application. Am Heart J 61:61-75,1961
- 29. Kaneko Z, Kotani H, Komuta K, Satomura S. Studies on peripheral circulation by "Ultrasonic Blood-Rheograph". Jpn Circ J 25:203-13,1961
- 30. Kaneko Z. First step in the development of the Doppler flowmeter. Ultrasound Med Biol 12:187-95,1986
- 31. Franklin DL, Schlegel W, Rushmer RF. Blood flow measured by Doppler frequency shift of backscattered ultrasound. Science 1961; 134: 564-5
- 32. Strandness DE, Schultz RD, Summer DS. Rushmer RF. Ultrasonic flow detection: A useful technique in the evaluation of peripheral vascular disease. Am J Srug 113:311-20,1967
- 33. Baker DW, Rubenstein SA, Lorch GS. Pulsed Doppler echocardiography: Principles and applications. Am J Med 63:69-80,1977
- 34. Brandestini MKE, Phillips DJ, Baker DW. Color digital echo/Doppler image presentation. Ultrasound Med Biol 7:21-31,1981
- 35. Namekawa K. Imaging of blood flow using autocorreleation. Ultrasound Med Biol 8(suppl.1):138,1982
- 36. Omoto R. Color atlas of real-time two-dimensional doppler echocardiography. Lea & Febiger, 1982
- 37. Omoto R, Yokote Y, Takamoto S, et al. The development of real-time two-dimensional Doppler echocardiography and its clinical significance in acquired valvular diseases with special reference to the evaluation of valvular regurgitation. Jpn Heart J. 25:325-40,1984
- 38. DuBose TJ, Baker AL. Confusion and direction in diagnostic Doppler sonography. J Diag Med Sonograph 25:173-7,2009
- 39. 河西千廣. 1983年:カラードプラ装置はどのようにして開発されたか. 日本超音波学会50周年記念誌. 19-21,2013
- 40. 吉川義博.カラードプラの開発. 第30回日本超音波学会講演会. 11-18,2005
- 41. Buschman W. New equipment and transducer for ophthalmic diagnosis. Ultrasonics 3:18-21,1965
- 42. 仁村泰治. 回想-超音波Doppler診断法の誕生外史. 第83回学術集会特別企画「私と超音波」119-22,2010
- 43. 金子仁郎. 超音波ドプラ血流検査法開発の回顧. Neurosonology 1:85-95,1988
- 44. 医用画像電子博物館 https://www.jira-net.or.jp/vm/
