- トロトラスト禍
- 造影剤トロトラストの特徴
- 原著論文
- 1928 新しい造影剤トロトラストの有用性
- トロトラスト誘発腫瘍
- 関連文献
- 1932 トロトラストの安全性に対する警告
- 原著論文
- 1947 トロトラスト誘発腫瘍の初報
トロトラスト禍
造影剤トロトラストの特徴

図1. トロトラストのアンプル.25%二酸化トリウム.血管造影,腎盂造影用,容量12ml.Die Chemische Fabrik von Heyden A.G., Radebeul の記載がある[15].
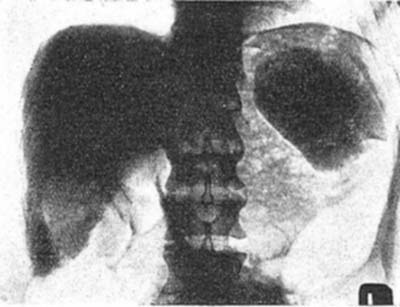
図2. トロトラスト静注による肝脾造影(hepatolienography).トロトラストが肝,脾に沈着し,高濃度に認められる.[2]
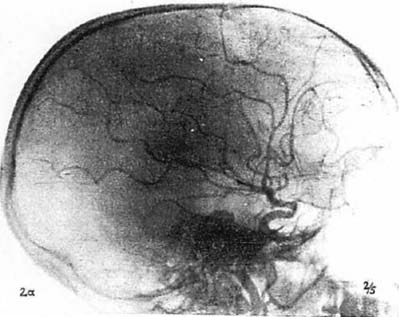
図3. トロトラストによる脳血管造影(前頭葉腫瘍例).それまでのヨード製剤と異なり血管痛がなく,コントラストも良好であった[3]
造影剤には原子番号の大きい元素が有利で,初期からさまざまな物質が試みられた.血管造影剤としては造影能,安全性の点からヨード(53I)が選択され,1920年代初頭より無機ヨード造影剤NaIが,1930年以降はUroselectanに代表される有機ヨード造影剤が臨床に供されたが,熱感など副作用が強く使いにくかった(→ 低浸透圧造影剤の開発).原子番号がさらに大きいトリウム(90Th)は,初期から造影剤の候補となり,1915年には硝酸トリウムによる腎盂造影の報告があるが,適当な製剤がなく普及しなかった[1].
1928年,ドイツの化学者Blühbaumらが二酸化トリウム(ThO2)コロイド溶液の有用性を報告した[→原著論文].この初報には気管支造影,膀胱造影などが供覧されているが,翌1929年には肝脾造影[2],脳血管造影[3],消化管造影[4]への応用が相次いで報告され,いずれもその有用性,安全性を高く評価するものであった.
製剤としては,ドイツのHeyden社からウンブラトール(Umbrathol),トロトラスト(Thorotrast)という商品名で販売された(図1).両者はいずれも25%二酸化トリウムコロイド溶液で,ウンブラトールは消化管造影用で粘膜面の描出に最適化されており,トロトラストは血管内投与,泌尿器造影用で血液,尿による凝集を低減した製剤であったが,基本的な性状は共通しており互換性があった[5].
トロトラストは,ヨードにくらべて造影能がきわめて良好で,ヨードで問題となる静脈内投与における熱感,刺激性がほとんど無いため急速に普及した*.トロトラストの大きな特徴は,血管内投与するとから細網内皮系に取り込まれて肝,脾,リンパ節,骨髄に沈着し,そのままほとんど排出されないことで,生物学的半減期は約400年と推定される.このため,静注24時間以後に腹部X線写真を撮影すると肝,脾が高濃度に描出され,これは 肝脾造影法(hepatolienography)と呼ばれた[2](図2).この他,脳血管造影にも広く使われた[3](図3).投与量は,例えば肝脾造影の場合,25mLを隔日3回[→関連文献],脳血管撮影では1回8~10mLであった[3].
* 1950年代にトロトラストの使用経験がある先輩医師から,あれほど使いやすい造影剤はなかった... という回顧談をきいた.実際に注入時の副作用がほとんどなく,造影能もきわめて良好であったという.低浸透圧ヨード製剤がまだなかった当時,トロトラストの危険性が指摘されてからもかなり長期にわたって使用され続けた一因に,このような背景があったものと思われる.
原著論文
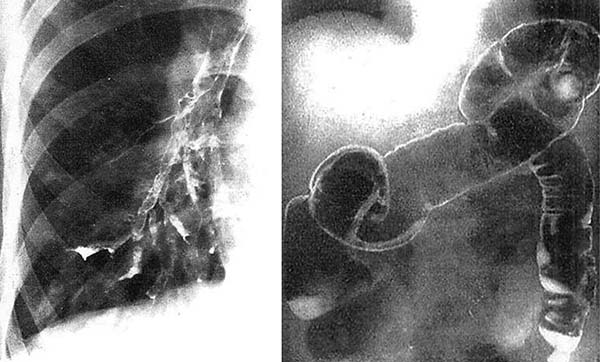
図4. トロトラストによる気管支造影,大腸造影
【要旨・解説】副作用の多いヨード造影剤にかわる造影剤として,特に粘膜面の描出を目的として,高濃度,持続性,温度安定性,無毒性,かつ低コストという条件を満足させるべく,コロイド物質の物理化学的性状を理論的に検討し,その理論に基づいて種々の物質を試験した.具体的にはヨウ化銀,水酸化セリウム,硝酸ビスマス,酸化ジルコニウム,二酸化トリウムであるが,二酸化トリウム(ThO2)がすべての条件を満足するものと考えられた.
副作用に関しては,粘膜⾯への腐⾷作⽤が最⼤の関⼼事となっており,多少の収斂作用があるとしている.後年大問題となるトリウムの放射能についてはひとこと触れられているだけで,トリウムが数ヶ⽉間存在しても組織への影響はなかったとして,ほとんど問題視されていない.
動物の気管支造影で安全性を確認し,また胃内投与にて血中に吸収されないことを確認した上で,ヒトの気管支造影を行ない,粘膜面の描出は良好であった.このほか,大腸,膀胱造影を試みているが,いずれも副作用はなかった.以上のことから,トリウム製剤は⾄適で安全な造影剤であると結論し,臨床例においてその造影能が優れていることを⽰している(図4).
トロトラスト誘発腫瘍
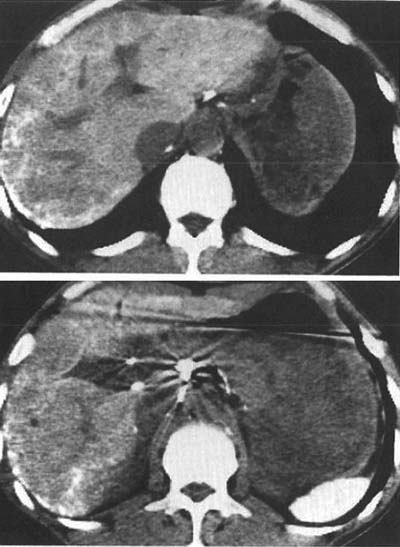
図5. トロトラスト投与39年後.沈着したトロトラストは,肝辺縁部に網目状の高吸収として認められる.肝門部のリンパ節,脾にも集積,高吸収があり,脾は高度に萎縮している.[13]
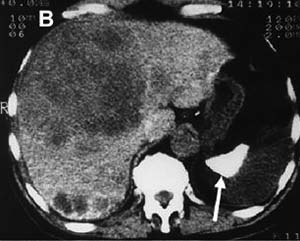
図6. 69歳男性.49年前,上肢骨折に対してトロトラストにて血管造影を施行,急性腹症にて発症.大きな低吸収の腫瘍があり(▲),その周囲にはトロトラスト沈着による網目状の高吸収が認められる.病理診断は血管肉腫. 脾の高吸収,高度萎縮(→)も認められる[9].
その優れた造影能と低刺激性から,発売直後より医師にも患者にも歓迎されたトロトラストであったが,その大きな特徴は,細網内皮系に取り込まれて肝脾,リンパ節などに長期,ほぼ恒久的に残留すること(図5),ならびに放射能を持つことである.天然に存在するトリウムは放射性同位体232Thのみで,半減期約140億年でα壊変して228Thとなる.当時,ラジウムを含む夜光塗料作業者の顎骨壊死,骨肉腫,いわゆる ラジウムガールズ事件 が既に知られており,これもα線による障害であったことから,トロトラストの安全性には当初より懸念がもたれた.既に1932年の時点で,米国医師会(AMA)はこれを指摘し,経静脈投与は認められないとしている[→関連文献].しかしその一方で,複数の論文が数年間にわたる多数症例のフォローアップの結果,安全であると報告しており[6,7],世界中で広く臨床に供されることになった.後から考えれば,この時点で放射線障害が認められなかったのは,単に腫瘍の潜伏期に比して観察期間が短か過ぎたためであった.
トロトラストの障害が初めて正式に報告されたのは,使用開始から約20年後の1947年のことである.肝梅毒腫(ゴム腫)診断目的のトロトラストによる血管造影後,12年を経て発症した肝内皮細胞肉腫の剖検例をMacMahornらが報告し,その因果関係を指摘した[→原著論文].その後も肝腫瘍,再生不良性貧血,白血病などの報告が相次ぎ,各国とも1950年代後半には次第に使用されなくなったが,1964年までに世界各国で10万人以上がトロトラストを投与された.その後の追跡結果は各国で報告されているが,例えばドイツの報告では1969~91年のフォロー期間中,トロトラストを投与された899例中410例に肝腫瘍が発生し,これに対して他の造影剤による検査を受けた対照群662例からの肝腫瘍は2例であった[8].日本の厚生省(当時)による調査でも,1966年までに124例のトロトラスト関連腫瘍が報告されている(肝肉腫が最多,潜伏期平均19.4年)[14,15].腫瘍発生までの潜伏期は16~45年とされるが,これに起因する腫瘍の発生は現在もなお続いている[9,10](図6).
トロトラストは70%が肝に集積し,誘発性腫瘍も肝に最も多い.特に胆管細胞癌,血管肉腫が特徴的であるが,肝細胞癌も発生する.トロトラストはKuppfer細胞に取り込まれて門脈域に主に集積する.ここから放出されるα線の飛程は短いが,沈着巣から範囲10μ近傍の被曝量は100Gy/年にもなり[11],門脈域周囲の細胞が特に障害されて胆管細胞癌,血管肉腫が多くなるものと考えられる.この他にも,胆嚢,肝外胆管,その他全身の悪性腫瘍の増加が知られている[12] .
関連文献
【要旨・解説】1932年,米国医師会(American Medical Association, AMA)の薬学化学審議会(Council on Pharmacy and Chemistry)が,その3年前に発売された造影剤トロトラストの安全性について検討し,機関紙JAMAに掲載した報告書である.
全般に使用者の評判は良いが,まだ具体的な症例報告など実証データを欠くことが指摘されている.急性副作用は報告されておらず安全と思われるが,長期的な副作用は不明である.特に静脈内投与では肝,脾,リンパ節などに蓄積して排出されないことから,体内に分布するトリウム量からα線の組織への影響を推定し,骨,歯牙病変を来たしうる既知のラジウム量に匹敵しうるとしている.現状では障害の報告はないが,夜光塗料作業者の職業病(いわゆるラジウムガールズ事件)では,障害が明らかとなったのは退職1~7年後であったことを考えると,まだ観察期間が不足していると述べ,審議会としては静脈内投与不認可の決定を下している.
先見の明に富む判断であったといえるが,現実にはこれ以後も静脈内投与が続けられ,多くの犠牲者を生む結果となった.
原著論文
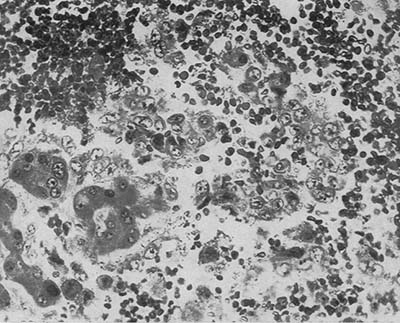
図7. 血液細胞に混じって腫瘍細胞巣が認められる.
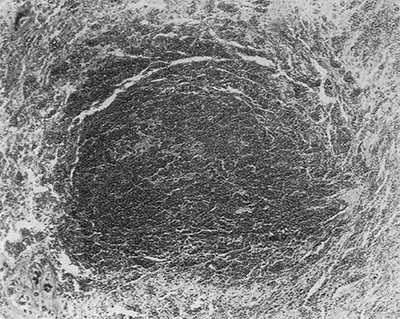
図8. 大きなトロトラスト沈着巣
【要旨】70歳⼥性.58歳時に肝の梅毒⾁芽腫(ゴム腫)の診断に際してトロトラストによる動脈造影が⾏なわれた既往があり,その12年後に出⾎性ショックで⼊院,死亡した.
病理所⾒で,肝内転移を伴う出血性の肝腫瘍が認められると同時に,肝内にトロトラスト沈着巣が多発していた(図7,図8).脾,リンパ節,骨髄にもトロトラスト沈着巣が認められた.最終診断は,「多発転移を伴う肝内皮細胞肉腫からの致死的腹腔内出血.肝,脾,リンパ節,骨髄,骨,副腎,腎,血管壁の変性を伴うトロトラスト沈着と放射線障害」 であった.
肝内の最も大きなトロトラスト沈着部位に接して腫瘍が認められた.ホルマリンに12ヵ月水浸した肝ブロック標本をガイガーカウンターで計測すると,トロトラスト沈着部位で最も放射能が強かった.ラジウムによる骨肉腫誘発の臨床例,動物実験例が報告されており,二酸化トリウムによる腹膜肉腫,皮下肉腫の動物実験例もあることから,トロトラストによって肝肉腫が発生したと考えられる.
【解説】トロトラストによる動脈造影の12年後に,肝⾁腫が発生し,その腫瘍内出⾎が原因と考えられた症例報告で,トロトラストと腫瘍の関係については推測の域を出ないが,組織所見および過去の報告を強力な状況証拠として論じ,その因果関係をほぼ断定したという点で画期的な論文である.ただし放射線障害の機序としてはγ線が最も有害であるとしているが,実際にはα線の影響が主である.前掲のBlühbaumの論文でトロトラストが紹介されてから約20年を経ており,これ以前にもトロトラストの腫瘍誘発性については議論されてきたが,潜伏期が長いためにその認識にこれだけの時間がかかり,その間に多くの犠牲者が生まれた.
出典
- 1. Burns JE. Thorium - A new agent for pyelography. J Am Med Assoc 64:2126-27,1915
- 2. Radt P. Eine neue Methode zur röntgenologischen Sichtbarmachung von Leber und Milz durch Injektion eines Kontrastmittels (Hepato-Lienographie). Med Klin 26:1888-91,1930
- 3. Moniz E, Pinto A, Lima A. Dir Vorzüge des Thorotrast bei arterieller Enzenpahlographie. Röntgenpraxis. 4:90-3,1932
- 4. Kalkbrenner H. Zur Frage des Reliefbildes am Dickdarm. Fortschr Geb Röntgenstr 36:693,1929
- 5. 村松篤治. 造影剤ウンブラトールならびにトロトラストの臨床的応用.グレンツゲビート 5:1133-54,1931
- 6. Rigler LG, Koucky RF, Abraham AL: Effects of thorium dioxide sol (Thorotrast) on human liver. Radiology 25:521-32,1935
- 7. Yater, WM, Coe FO, Ten years' experience with thorotrast hepatosplenography. Ann Intern Med 18:350-66,1943
- 8. Van Kaick G, Wesch H, Luhrs H, et al. Neoplastic diseases induced by chronic alpha-irradiation- Epidemiological, biophysical and clinical results of the German Thorotrast Study. J Radiat Res 32:20-33,1991
- 9. Takekawa S. Ueda Y, Hiramatsu H, et al. History note: tragedy of Thorotrast. Jpn J Radiol 33:718-22,2015
- 10. 谷木信仁, 中本伸宏, 吉田文他.ラジオ波焼灼療法により良好な病勢制御が得られた トロトラスト沈着症による肝内胆管癌の一例. 肝臓 61:262-9,2020
- 11. Kato Y. Alpha-ray dosage near thorotrast aggregate, Jpn J Radiol 26:1574-56,1967
- 12. Lipshutz GS, et al. Thorotrast-induced liver neoplasia: A collective review. J Am Coll Surg 195:713-8,2002
- 13. 佐々木文雄,木戸長一郎. トロトラスト肝におけるトロトラスト沈着粒子の経時的変化のX線学的検討. 日医放会誌 48:1333-31,1988
- 14. 大河原重之. Thorotrastの研究.第7報. Thorotrastによる発癌について. 日本医学放射線学会誌. 25:1231-37,1966
- 15. 金子昌生. トロトラストの歴史と低線量長期被ばくの教訓. Isotope News 677:20-22,2010
